อะตอม คือหน่วยที่เล็กที่สุดของสสารที่ยังคงสภาพความเป็นสสารอยู่ได้แบบจำลองอะตอม ตามทฤษฏี มีอยู่ 5 แบบ คือ
1. แบบจำลองอะตอมของดอลตัน
สสารทุกชนิดประกอบด้วยอนุภาคที่เล็กที่สุดเรียกว่า อะตอม ซึ่งไม่สามารถแบ่งแยกต่อไปได้อีก
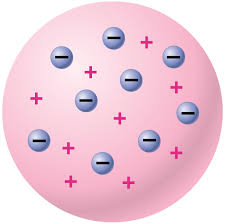
 2. แบบจำลองอะตอมของทอมสัน
2. แบบจำลองอะตอมของทอมสัน
- ค้นพบอิเล็กตรอน ที่ มีประจุไฟฟ้าลบ มีมวลประมาณ1/2000 ของมวลของ H
- โดยศึกษาพฤติกรรมของ หลอดรังสีแคโทด ในสนามแม่เหล็กไฟฟ้า
พันธะเคมี
แรงยึดเหนี่ยวทางเคมี
ในชีวิตประจำวันทั่วๆไปจะพบว่าสารชนิดหนึ่งๆมักจะอยู่รวมกันเป็นกลุ่มก้อนและเมื่อต้องการทำให้แยกออกจากกันจะต้องใช้พลังงานจำนวนหนึ่งตัวอย่างเช่น
1. เมื่อให้ความร้อนแก่สารจนกระทั่งโมเลกุลของสารมีพลังงานสูงพอจะทำให้เกิด
การเปลี่ยนสถานะ น้ำแข็ง (ให้พลังงานความร้อน) เปลี่ยนสถานะเป็น น้ำ(ของเหลว) ให้พลังงานความร้อน เปลี่ยนสถานะเป็น ไอน้ำ
สารบางชนิดอาจแยกสลายออกเป็นสารหลายชนิดได้
2. เมื่อให้พลังงานไฟฟ้าโมเลกุลของสารบางชนิดจะสลายตัวให้ธาตุที่เป็นองค์ประกอบ เช่นการแยกน้ำด้วยไฟฟ้า
จากข้อมูลข้างต้น แสดงว่ามีแรงยึดเหนี่ยวระหว่างโมเลกุล และแรงยึดเหนี่ยวระหว่างอะตอมที่เป็นองค์ประกอบของโมเลกุล
เราสามารถแบ่งแรงยึดเหนี่ยวออกเป็น 2 ประเภทดังนี้
1. แรงยึดเหนี่ยวภายในโมเลกุล (พันธะเคมี) อะตอม - อะตอม ได้แก่
พันธะโคเวเลนต์ (covelent bond)
พันธะไอออนิก (ionic bond)
พันธะโลหะ (metallic bond)
อ่านต่อ
